
سوربیتول چیست؟
بهمن 6, 1398
کلر و موارد مصرف آن
بهمن 6, 1398اسید سیتریک که به جوهر لیمو معروف است از جمله اسیدهای آلی که به وفور در لیموترش و پرتقال وجود دارد. فرمول شیمیایی اسید سیتریک C6H8O7 می باشد. اسید سیتریک یک هیدروکسی اسید است.
اسامی دیگر اسید سیتریک :
جوهرلیمو، اسید لیمو، سیتریک اسید، hydroxypropane، citric acid.
انواع اسید سیتریک :
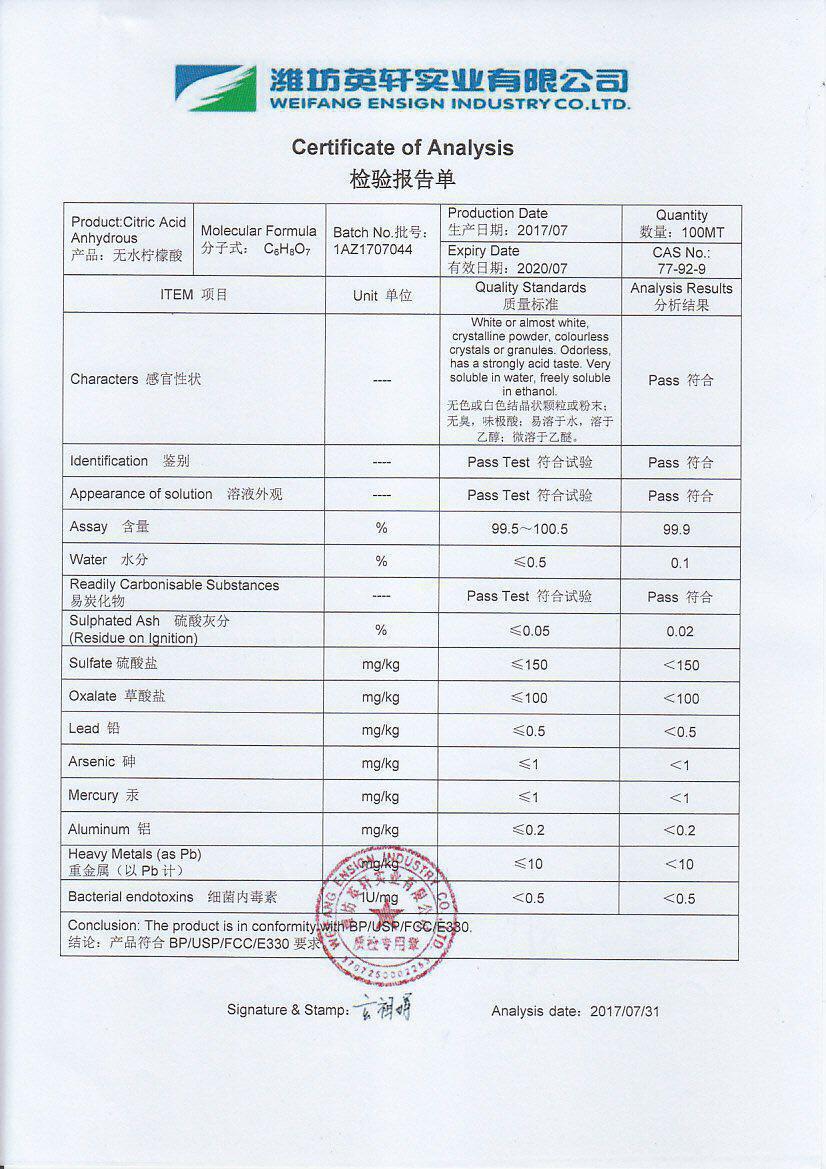
1. اسید سیتریک خشک (اسید سیتریک آنهیدروز)
2. اسید سیتریک آبدار (اسید سیتریک مونوهیدرات)
خلوص :
اسید سیتریک 98 درصد.
تعریف اسید سیتریک :
اسید سیتریک که به جوهر لیمو معروف است از جمله اسیدهای آلی که به وفور در لیموترش و پرتقال وجود دارد. فرمول شیمیایی اسید سیتریک C6H8O7 می باشد. اسید سیتریک یک هیدروکسی اسید است. هیدروکسی اسید گروهی از اسیدهای کربوکسیلیک هستند که یک گروه عاملی هیدروکسیل به آنها افزوده شده است.
از عمده ترین کشورهای تولید کننده آن کشور چین می باشد. از این اسید در صنایع نوشابه، آبلیمو و آرایشی بهداشتی و داروئی استفاده عمده دارد و علاوه بر طعم دهندگی باعث تنظیم ph می شود. اسید سیتریک دارای انواع خشک (آن هیدروز) و آبدار (مونوهیدرات) به صورت پودر کریستال تولید شده و در کیسه های کاغذی و چند لایه بسته بندی می گردد و به فروش می رسد.
کربوکسیلیک اسید :
کربوکسیلیک اسیدها، دسته ای از ترکیبات آلی هستند که در ساختار خود دست کم یک گروه عاملی کربوکسیل دارند. در این گروه عاملی، یک گروه هیدروکسیل به یک گروه کربونیل پیوسته است. چون گروه کربونیل، الکترون کشنده است پیوند O-H به اندازه ای قطبیت دارد که هیدروژن آن می تواند در محلول آبی به صورت یون H+ از مولکول اسید جدا شود.
قدرت اسیدی قوی ترین کربوکسیلیک اسیدها غیر آلی قوی مانند سولفوریک اسید، نیتریک اسید، هیدروکلریک اسید بسیار کمتر است و هیچ یک از اسیدهای آلی، اسید قوی به شمار نمی رود.
خواص اسید سیتریک :
اسیدیته اسید سیتریک ناشی از سه گروه کربوکسی است که می توانند پروتون از دست دهند. یون سیتریک اسید، سیترات می باشد. سیترات ها بافرهای خوبی برای کنترل ph محلول های اسیدی هستند. یون سیترات با بسیاری از فلزات نمک سیترات ایجاد می کند که مهمترین آن سیترات کلسیم می باشد که برای نگهداری غذا از فساد و خوش طعم کردن آن بکار می رود. یون سیترات می تواند با فلزات ترکیبات کی لیتی ایجاد کند.
در دمای اتاق اسید سیتریک، پودر سفید رنگ کریستالی می باشد که در دو نوع بی آب و آبدار وجود دارد. سیتریک بی آب (خشک) از کریستالیزه شدن اسید سیتریک در آب گرم ایجاد می شود در حالی که فرم آبدار از تبلور آن در آب سرد بوجود می آید. فرم آبدار آن با حرارت دادن در 47 درجه سانتی گراد به نوع خشک تبدیل می شود. اسید سیتریک در حرارت بالای 175 درجه تجزیه شده و CO2 و آب آزاد می شود.
تاریخچه اسید سیتریک :
اسید سیتریک در قرن هشتم توسط جابربن حیان کشف شده است. دانشمندان قرون وسطی در قرن 13 با خواص اسیدی لیمو آشنا شدند. اسید سیتریک برای اولین بار توسط شیمیدانی سوئدی کارل ویلمام در سال 1784 توسط متبلور کردن آبلیمو جداسازی شد.
در سال 1893 C.wehner با کشف کپک پنی سیلیوم توانست اسید سیتریک را توسط شکر تولید کرد. تولید میکروبیولوژیکی اسید سیتریک تا جنگ جهانی اول روش صنعتی مهمی کشف کرد که در تولید سیتریک کارآمد بودند. بیشتر اسید سیتریک تولیدی جهان با روش استفاده از کپک اسپرژیل انجام می گیرد.
تولید اسید سیتریک :
در روش تولید سیتریک اسید توسط کپک اسپرژیل، این کپک را روی شکر کشت می دهند تا اسید سیتریک تولید کند. بعد از جدا کردن از محلول حاصل، سیتریک را توسط ته نشین کردن با آب آهک به صورت نمک سیترات کلسیم جدا سازی می کنند. سیترات کلسیم در حضور اسید سولفوریک، اسید سیتریک تولید می کند.
موارد مصرف و کاربرد اسید سیتریک :
اسید سیتریک در بسیاری از صنایع کاربرد دارد :
1. ماده محافظ مواد غذایی.
2. سیتریک به عنوان چاشنی غذا.
3. نمک های سیترات با فلزات گوناگون در افراد بیمار به هنوان کمک های غذایی مورد استفاده است.
4. دارای خواص بافری در کنترل ph در مواد تمیزکننده خانگی.
5. به دلیل توانایی تشکیل کیلیت با فلزات در ترکیب شوینده ها.
6. داروسازی.
7. به عنوان ماده بی خطر برای مصرف در غذاها.
8. صنعت نوشابه و آبمیوه.


3 Comments
مطلبتون درباره اسید سیتریک خیلی خوب بود ممنون
فکر نمیکردم تا این حد کاربردی باشه این محصول
ممنون بله اسید سیتریک بسیار کاربردی و مفید هست
همواره موفق باشید